:: ‘teste rápido de Zika’
Ministério da Saúde vai distribuir teste rápido de Zika produzido pela Bahiafarma

O Ministério da Saúde anunciou, nesta terça-feira (25), a compra de 3,5 milhões de testes rápidos para identificar o vírus Zika. Está prevista a distribuição de dois milhões de kits até o final deste ano e o restante até fevereiro de 2017. A tecnologia confirma, em 20 minutos, se o paciente está ou já foi infectado pelo vírus Zika em algum momento da vida. Ou seja, com a tecnologia será possível identificar o vírus no organismo, independente do tempo de infecção. A produção do insumo será feita pelo laboratório público Bahiafarma. Atualmente, o teste ofertado no Sistema Único de Saúde (SUS) é o PCR (biologia molecular), que só detecta a doença durante o período de viremia, quando o vírus está presente na corrente sanguínea. O Ministério da Saúde investiu R$ 119 milhões para a aquisição dos testes sorológicos, com projeção para garantir o abastecimento da rede por doze meses. A negociação com a Bahiafarma permitiu a compra no valor unitário de R$ 34,00, quase quatro vezes menor que o valor proposto por outra empresa do mercado, de R$ 131,75 por teste.
 A compra foi feita por meio de licitação dispensável, quando é permitida à administração pública a contratação de produtos ou serviços em que a transferência de tecnologia é estratégica ao SUS. A medida está prevista na Lei nº 8.666/93. O desenvolvimento do teste rápido de diagnóstico de infecção pelo vírus Zika é fruto da parceria entre o Governo da Bahia e a empresa sul-coreana Genbody Inc., que firmaram um acordo de transferência de tecnologia para a Bahiafarma.
A compra foi feita por meio de licitação dispensável, quando é permitida à administração pública a contratação de produtos ou serviços em que a transferência de tecnologia é estratégica ao SUS. A medida está prevista na Lei nº 8.666/93. O desenvolvimento do teste rápido de diagnóstico de infecção pelo vírus Zika é fruto da parceria entre o Governo da Bahia e a empresa sul-coreana Genbody Inc., que firmaram um acordo de transferência de tecnologia para a Bahiafarma.
Bahiafarma obtém registro para teste rápido de Zika inovador no mercado
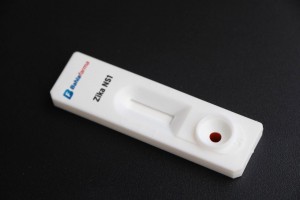 A Bahiafarma, laboratório público do Estado da Bahia, obteve o registro da Agência Nacional de Vigilância Sanitária (Anvisa) para produção e distribuição do teste rápido de detecção de Zika vírus a partir da identificação do antígeno NS1 na corrente sanguínea do paciente. Trata-se de um dispositivo capaz de realizar o diagnóstico da doença a partir do primeiro dia de infecção, preenchendo uma lacuna não coberta pelos demais exames disponíveis hoje no mercado.
A Bahiafarma, laboratório público do Estado da Bahia, obteve o registro da Agência Nacional de Vigilância Sanitária (Anvisa) para produção e distribuição do teste rápido de detecção de Zika vírus a partir da identificação do antígeno NS1 na corrente sanguínea do paciente. Trata-se de um dispositivo capaz de realizar o diagnóstico da doença a partir do primeiro dia de infecção, preenchendo uma lacuna não coberta pelos demais exames disponíveis hoje no mercado.
O teste rápido Zika NS1 da Bahiafarma, mais um fruto do acordo tecnológico firmado entre a empresa baiana e o laboratório sul-coreano GenBody, é o primeiro dispositivo do gênero feito por um laboratório oficial brasileiro. Por meio dele, é possível confirmar o contágio tão logo surjam os sintomas, o que torna mais ágil a aplicação de tratamentos adequados, eliminando a possibilidade de diagnósticos inconclusivos. O teste demanda uma pequena quantidade de sangue do paciente e fornece o resultado em até 20 minutos.
Teste rápido de Zika da Bahiafarma supera expectativas em avaliação do Ministério da Saúde
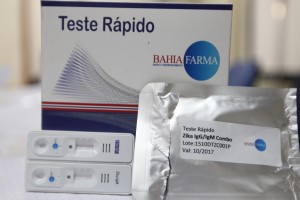 Submetido à rigorosa avaliação do Instituto Nacional de Controle de Qualidade em Saúde (INCQS), órgão ligado ao Ministério da Saúde, o teste rápido para detecção de Zika vírus da Bahiafarma obteve um dos melhores resultados já registrados para dispositivos do gênero no mundo.
Submetido à rigorosa avaliação do Instituto Nacional de Controle de Qualidade em Saúde (INCQS), órgão ligado ao Ministério da Saúde, o teste rápido para detecção de Zika vírus da Bahiafarma obteve um dos melhores resultados já registrados para dispositivos do gênero no mundo.
O kit do laboratório público baiano registrou índices de 97% de sensibilidade e 96% de especificidade para infecções recentes (IgM) e de 100% de sensibilidade e 98% de especificidade para infecções mais antigas (IgG). “O resultado corrobora a avaliação feita pela Anvisa [Agência Nacional de Vigilência Sanitária], que já havia aprovado o dispositivo, ao publicar o registro para sua produção e distribuição, no fim de maio”, afirma o diretor-presidente da Bahiafarma, Ronaldo Dias.
O secretário da Saúde do Estado, Fábio Vilas-Boas, destaca que, “com mais essa avaliação positiva, confirmamos nosso compromisso de fornecer ao Sistema Único de Saúde (SUS) e à população produtos de primeira linha para a saúde pública brasileira”. Vilas-Boas acrescenta “o compromisso do governador Rui Costa em apoiar o investimento em pesquisa e tecnologia com o parceiro internacional da Bahiafarma, o laboratório coreano Genbody”.
Segundo o subsecretário de Saúde da Bahia, Roberto Badaró, os resultados obtidos pelo teste rápido de Zika vírus da Bahiafarma são “excepcionais”. “Um dos melhores testes rápidos do mundo, o de HIV de quarta geração, tem acurácia de 95%, e testes para diversas outras doenças, como sífilis e hepatite, registram abaixo de 85%”, justifica Badaró, que é professor titular de Infectologia da Universidade Federal da Bahia (Ufba) e da Universidade da Califórnia, em São Diego (EUA).
Com a aprovação do INCQS, o teste rápido de Zika vírus da Bahiafarma está liberado para aquisição, por parte do Ministério da Saúde, e distribuição pelo SUS em todo o País. Estima-se que a demanda do SUS pelo dispositivo seja de 500 mil testes por mês – montante que a Bahiafarma está apta a produzir em 30 dias, bastando a ordem de compra ser emitida pelo ministério.
O resultado reforça a posição da Bahiafarma como centro indutor de desenvolvimento das indústrias farmacêutica, farmoquímica e biotecnológica na Bahia e no Nordeste, inserindo o estado na vanguarda da produção de insumos para a saúde no Brasil e fortalecendo a descentralização do Complexo Industrial da Saúde. (Foto: Alberto Coutinho/GOVBA)
Ministério da Saúde avalia teste rápido do Zika Vírus produzido na Bahia

Na manhã desta segunda-feira (13), o ministro da Saúde, Ricardo Barros, visitou a capital baiana para conhecer o teste sorológico rápido de identificação do Zika Vírus, desenvolvido pelo Governo do Estado, por meio da Fundação Baiana de Pesquisa Científica e Desenvolvimento Tecnológico (BahiaFarma), em parceria com o Senai-Cimatec. Acompanhado do vice-governador, João Leão, e do secretário estadual da Saúde (Sesab), Fábio Vilas-Boas, o ministro avaliou o produto e falou sobre as intenções do governo federal em utilizar a iniciativa nacionalmente, no Sistema Único de Saúde (SUS).
De acordo com o ministro Ricardo Barros, assim que forem realizados todos os procedimentos, será efetuada, junto à BahiaFarma, compra de grande volume dos testes, que estarão disponíveis pelo SUS. “Nós vamos aguardar a negociação de preço, ver o volume que podemos comprar e vamos estabelecer a população em situação de risco que receberão prioridade. A população de risco será atendida em primeiro lugar. Desde já, é importante que tenhamos a capacidade de atender as mulheres em idade fértil e gestantes, por causa dos riscos de má formação congênita e microcefalia relacionados ao vírus. São iniciativas como essa que demonstram a qualidade do nosso corpo científico que desenvolvem tecnologia no Brasil”, destacou o ministro.
 O teste rápido permite detectar se o paciente está com a doença ou se já foi infectado há mais tempo pelo vírus. O exame utiliza uma pequena amostra de soro do paciente e fornece os resultados em até 20 minutos. O aparelho do exame é composto por dois dispositivos portáteis (7×2 cm cada). Um deles reage à imunoglobulina M (IgM) – das infecções de até duas semanas, e o outro à imunoglobulina G (IgG) – infecção com tempo superior a duas semanas. Já registrado pela Agência Nacional de Vigilância Sanitária (Anvisa), agora o teste passará por avaliação de qualidade.
O teste rápido permite detectar se o paciente está com a doença ou se já foi infectado há mais tempo pelo vírus. O exame utiliza uma pequena amostra de soro do paciente e fornece os resultados em até 20 minutos. O aparelho do exame é composto por dois dispositivos portáteis (7×2 cm cada). Um deles reage à imunoglobulina M (IgM) – das infecções de até duas semanas, e o outro à imunoglobulina G (IgG) – infecção com tempo superior a duas semanas. Já registrado pela Agência Nacional de Vigilância Sanitária (Anvisa), agora o teste passará por avaliação de qualidade.
Segundo o titular da Sesab, o processo de autorização do Ministério tem recebido prioridade e algumas etapas legais ainda precisam ser vencidas para a absorção do teste e incorporação pelo SUS. “Esse é um processo junto ao Ministério que já dura seis meses. Assim que for aprovado, temos condições de fornecer, de imediato, 100 mil testes rápidos. A nossa capacidade de produção é de até 500 mil unidades do exame, mensalmente, o que atende à demanda nacional. Ainda assim, solicitamos ao Ministério da Saúde recursos na ordem de R$ 7 milhões para investir na produção e ampliar ainda mais a nossa capacidade”, explicou Vilas-Boas. (Fotos: Camila Souza/GOVBA)
- 1


















